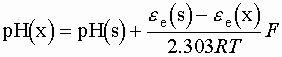
VÁLASZOK
pH mérése hidrogénelektróddal
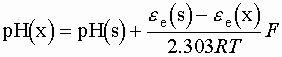
![]()
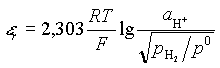
Félig telített (1/2t) és telített (t) KCl-oldattal is mérjük az egyensúlyi potenciált. Az elektródreakció potenciálja a következő összefüggéssel közelíthető:
e r= e 1/2t + 2(e t - e 1/2t) = e t + (e t - e 1/2t)
Megjegyzés:
1. A referenciaelektród (telített kalomelelektród) elektródreakció potenciálja: +0,240 V , így biztosak lehetünk, hogy 0-14 pH között a hidrogénelektród a negativ pólus, ezért h elkövetése elvileg is pótolható.
2. A hidrogéngáz parciális nyomása a standard és ismeretlen oldat esetén ugyanaz, ezért a légköri nyomás pontos ismerete nem szükséges.