Az elektrolízis tanulmányozása
Eszközök
(Az EF421 potenciosztát
használatának leírása itt található.)
FIGYELEM
A mérés elvégzéséhez szükséges
elméleti ismeretek egy része a vegyészek számára készített „Az elektromotoros
erő mérése; galváncellák tanulmányozása” című mérési leírásban szerepel. (A
benne szereplő fontosabb fogalmak: elektródpotenciál, elektródreakció,
csereáram sűrűség; elsőfajú és másodfajú elektródok, redoxi elektródok; Nernst
egyenlet; galváncella, celladiagram, cellareakció, cellareakció potenciálja,
elektromotoros erő, kapocsfeszültség, cella belső ellenállása; Daniell elem,
Weston-féle normálelem, referenciaelektródok)
Ez a
leírás pdf formátumban letölhető (sőt letöltendő,
mert számonkérésnél ismertnek tételezzük fel!) a következő helyről: http://foundation01.chem.elte.hu/Vegyesz_III/01_BLOKK/
Az elektródreakció potenciálja
annak a galváncellának a cellareakció potenciálja, amelynek diagramjában a bal
oldalon a standard hidrogénelektród, jobb oldalán pedig a vizsgált elektród
van.
Egyszerű elektródnak nevezzük az olyan
elektródot, amelyen csak egyetlen elektródreakció zajlik le. Keverékelektród az olyan elektród, amelyen
egynél több elektródreakció megy végbe.
Anódnak nevezzük azt az
elektródot, amelyen az átfolyó eredő áram pozitív (pozitív az áram, ha a
pozitív töltések az elektronvezetőből az ionvezetőbe áramlanak). Az anódon
kizárólagosan (vagy túlnyomó részben) oxidáció zajlik le. Katódnak
nevezzük azt az elektródot, amelyen az átfolyó eredő áram negatív. Az katódon
kizárólagosan (vagy túlnyomó részben) redukció zajlik le.
Az elektród árammentes állapotában
mért, időben állandósult elektródpotenciálját nyugalmi
potenciálnak (e ny) nevezzük. Egyszerű
elektród esetén a nyugalmi potenciál
egyben egyensúlyi potenciál is (e ny = e e). Keverékelektród esetén a nyugalmi
potenciál keverékpotenciál. Ez lehet egyensúlyi potenciál vagy
stacionárius potenciál. Az áramsűrűség mindkét esetben nulla, de a második
esetben nem áll fenn az elektródon végbemenő minden folyamatra egyensúly.
Ha a galváncellát nem áramtermelésre, hanem kémiai anyagok elektromos
árammal történő átalakítására használjuk, a berendezést elektrolizálócellának,
a végbemenő folyamatot elektrolízisnek nevezzük.
Az elektród potenciálja a nyugalmi
potenciálhoz képest külső hatásra megváltozhat. Ez a jelenség a polarizáció.
Ekkor az elektródon elektromos áram halad át. A polarizált elektród
elektródpotenciálját polarizációs potenciálnak (e p) nevezik.
Ha a polarizált elektród katódként működik, akkor katódos
polarizációról, ha anódként, akkor anódos
polarizációról beszélünk. A polarizációs potenciál és az egyensúlyi
potenciál különbsége a túlfeszültség (h ): h = e p - e e.
Az e (I),
I(e ), h (I)
és I(h )
függvényeket leíró görbéket polarizációs görbéknek
nevezzük. Polarizációs görbéket két módszerrel határozhatunk meg. Galvanosztatikus
(galvanodinamikus) módszer esetén a vizsgált elektródon az áramot állítjuk
be (meghatározott program szerint változtatjuk) és mérjük a kialakuló
potenciált. Potenciosztatikus (potenciodinamikus)
módszer esetén a vizsgált elektródon a potenciált állítjuk be (meghatározott
program szerint változtatjuk) és mérjük az kialakuló átfolyó áramot. A modern potenciosztátok mindkét módszerrel képesek dolgozni.
A polarizációs potenciált és a túlfeszültséget rendszerint ún. háromelektródos cellában mérik. A vizsgált
elektród az ún. munkaelektród (jele M [munka], W [working]). M és az áramvezető
segédelektród (jele:S [segéd], C [counter] vagy A [auxiliary]), között
áram folyhat a cella külső áramkörében. M potenciálját az összehasonlító
elektróddal (jele R [referencia]) szemben mérik. M és R között gyakorlatilag
nem folyik áram. Az összehasonlító elektród összekötő csövét kapillárissá
vékonyítják (Luggin-kapilláris) és a munkaelektród
felületéhez közel helyezik el, hogy az ohmikus potenciálesést, így a
potenciálmérés bizonytalanságát csökkentsék.
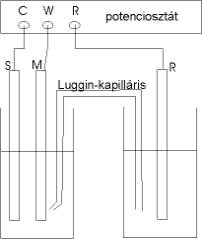
Háromelektródos
cella rajza
A gyakorlatban fontos a cella azon minimális elektromos potenciálkülönbségének az ismerete, amelynél nagyobb feszültségnél már a kívánt cellareakció játszódik le (és tartósan a maradékáramnál nagyobb áram mérhető). Ezt a minimális feszültséget bomlásfeszültségnek nevezik. Az egyes elektródok potenciáljai ekkor a leválási potenciálok. A bomlásfeszültség és a leválási potenciál nem pontosan definiált mennyiségek, ezért a laboratóriumi gyakorlat során ezeket nem számoljuk.
Egy elektródfolyamat az alábbi sorozatosan egymás után következő lépésekből áll:
1. Anyagszállítás az elektrolit belsejéből az oldatnak az elektróddal érintkező rétegébe
2. Az elektródfolyamatban résztvevő ionok elhelyezkedése a kettősréteg fémmel közvetlenül érintkező rétegében. (adszorpció)
3. Ionok vagy molekulák kemiszorpciója a felületen.
4. Elektrokémiai reakció (töltésátlépés)
5. Primer termékek adszorpciója
6. Primer termékek deszorpciója
7. Primer termékek szekunder átalakulása kémiai reakcióval.
8. Végtermék eltávozása a felületről.
Reakciókinetikai tanulmányaink alapján tudjuk, hogy a bruttó folyamat sebességét mindig az energetikailag leginkább gátolt részfolyamat szabja meg.
Az elektrokémiai reakciók sebességét az áramsűrűséggel szokás kifejezni:
j = zFv, ahol z az elektródreakció töltésszáma F a Faraday-állandó, v a reakció sebessége
Nézzük meg, mitől függ az áramsűrűség nagysága a két legfontosabb esetben:
·
ha a töltésátlépés a gátolt részfolyamat
(“átlépési polarizáció”)
![]()
ahol j0 a csereáram-sűrűség, a átlépési tényező, h a
túlfeszültség
Ez az Erdey-Grúz-Volmer egyenlet.
·
ha a diffúzió a gátolt részfolyamat
(“diffúziós polarizáció”)
![]() , ahol
, ahol
ni az i-edik komponens sztöchiometriai száma, Di
az elektródfolyamatban résztvevő i-edik komponens diffúziós
együtthatója, ci,0 az i-edik anyag
koncentrációja az elektród felületénél, ci,∞
az oldat belsejében, di az ún. Nernst-féle diffúziós réteg vastagsága.
A forgó korongelektród
Ha az elektródfém olyan fémkorong, amely
középpontján átmenő és síkjára merőleges tengely körül forog, akkor a
felülethez közeli folyadékréteget a centrifugális erő a korong kerülete felé
hajtja. Kimutatható, hogy a diffúziós réteg di vastagsága lamináris áramláskor a forgó
korong egész felületén állandónak adódik. Következésképpen a diffúzió által
megszabott áramsűrűség is azonos a forgó korongelektród minden részén.
A diffúziós réteg vastagsága a forgó
korongon:
![]() , ahol Di
az i-edik diffundáló részecske diffúziós együtthatója, n az oldat kinematikai viszkozitása, w a korong forgásának szögsebessége.
, ahol Di
az i-edik diffundáló részecske diffúziós együtthatója, n az oldat kinematikai viszkozitása, w a korong forgásának szögsebessége.
A diffúzió által fenntartott áramsűrűség
![]()
A fenti egyenletből látható, hogy az adott
elektródon mérhető áram arányos a korong forgási sebességének négyzetgyökével.
Amennyiben minden más feltételt állandóan tartunk, könnyedén eldönthetjük, hogy
az általunk vizsgált folyamat diffúziókontrollált vagy sem.
Ajánlott irodalom:
Kiss László: Bevezetés az elektrokémiába
A vegyész 1.sz blokk „Az
elektromotoros erő mérése; galváncellák tanulmányozása.” c. mérés
leírása
Feladat: Az elektrolízis tanulmányozása polarizációs görbék felvételével.
Figyeljük
meg
•
0,5 mol/dm3 koncentrációjú H2SO4-oldatban
az oldott oxigén redukcióját külünböző fordulatszámokon;
•
az oxigén kiűzésének (oxigénkoncentráció
csökkenésének) hatását egy adott fordulatszámon.
•
0,5 mol/dm3 koncentrációjú H2SO4-oldatban
a hidrogén (H+-ionok) leválását;
•
az eddig használt 0,5 mol/dm3
koncentrációjú H2SO4-oldatban (szilárd KCl, KBr és KI só
adagolása után) a halogenid ionok leválását adott fordulatszámon.
A gyakorlaton potenciodinamikus elektrolízist végzünk háromelektródos cellában. Munkaelektródnak platina korong elektródot, áramvezető segédelektródnak szénrudat használunk, referenciaelektródunk telített kalomelelektród. A munkaelektród és a referenciaelektród közötti oldat ellenállásának csökkentésére a referenciaelektród terét Luggin-kapillárissal vezetjük a munkaelektródhoz. Figyeljünk, hogy a kapillárist ne törjük el! A polarizálást EF421 típusú potenciosztáttal végezzük. A kezdeti potenciált, a méréshatárt, a potenciálváltoztatás irányát és a polarizálási sebességet manuálisan kell beállítani. Az adatok gyűjtését a potenciosztát analóg potenciál- és áramkimenetéről AD-konverter és interfész segítségével számítógép végzi. Az adatgyűjtő program indítása az elz.bat batch-file futtatásával történik, de általában a számítógép indítása után automatikusan elindul.
A telített kalomelelektród egyensúlyi potenciálja 0,240 V a standard hidrogénelektródhoz képest.
A munkaelektródot már a forgatóba befogva találjuk. A cellából öntsük ki a vizet, majd töltsünk bele 200cm3 kénsavoldatot, az oktató segítségével szereljük össze a cellát. A Luggin-kapilláris csapját a vizsgálandó oldatba mártjuk (vagy cseppentővel megnedvesítjük) a csap ellenállásának csökkentése érdekében. A referenciaelektródot tartalmazó főzőpohárba is a vizsgálandó kénsavoldat kerüljön. A mérés megkezdése előtt kb. 10 percig buborékoltassunk át levegőt az oldaton, hogy az levegővel telített legyen. A levegővel telített oldatban ezután polarizációs görbéket veszünk fel az alábbi táblázatban található körülmények között, különböző fordulatszámokon. Miután ezzel végeztünk, megvizsgáljuk az oxigén kiűzésének hatását a polarizációs görbékre: N2 gázt vezetünk át a cellán és polarizációs görbéket veszünk fel adott fordulatszámon mindaddig, míg változást tapasztalunk. Ezután az oxigénmentesnek tekinthető elektrolitban megfigyeljük a H+ ionok leválását. A pontos potenciálintervallumot és egyéb adatokat szintén a táblázatban találhatjuk meg.
Végül néhány cm3
0,5 mol/dm3 koncentrációjú H2SO4-oldatban feloldunk
0,030g KCl-ot, 0,065g KBr-ot és 0,020g KI‑ot, majd a kész oldatot a
cellába töltjük. A megadott mennyiségeknél többet semmi esetre se oldjunk fel!
A reduktorban maradt N2-gázzal az oldatot összekeverjük, majd polarizációs görbét veszünk fel a táblázatban található
beállításokkal.
|
Sorsz. |
Mérés
előtti ill. közbeni teendő |
Induló
potenciál |
Végpotenciál |
Polarizáció
sebessége / (mV/min.) |
Méréshatár
/ mikroamper |
Forgás
sebessége (kijelzett értéke / fordulatszám/perc) |
|
1. |
Mérés
előtt levegő |
500mV |
hidrogénfejlődés,
kb. –250mV |
250 |
20 |
0 / 0 |
|
2. |
|
500mV |
hidrogénfejlődés,
kb. –250mV |
250 |
200 |
5 / 240,4 |
|
3. |
|
500mV |
hidrogénfejlődés,
kb. –250mV |
250 |
200 |
10 /
484,4 |
|
4. |
|
500mV |
hidrogénfejlődés,
kb. –250mV |
250 |
200 |
20 /
971,8 |
|
5. |
|
500mV |
hidrogénfejlődés,
kb. –250mV |
250 |
200 |
30 / 1460 |
|
6. |
Mérés
alatt N2 |
500mV |
hidrogénfejlődés,
kb. –250mV |
600 |
200 |
10 /
484,4 |
|
7. |
Mérés
előtt szilárd halogenid adagolás |
0.2V |
1.25V |
60 |
200 |
10 /
484,4 |
A polarizáció iránya oxigénredukció és H+-ion leválás esetén – (katódos polarizáció), a halogenidek esetén + (anódos polarizáció). A polarizációs görbéket számítógépes adatgyűjtéssel regisztráljuk.
A mérés végén az elektródot polarizáljuk negatív potenciálra (enyhe hidrogénfejlődés), hogy a halogenid ionok deszorbeálódjanak. A munkaelektródot vízzel jól öblítsük le, itassuk szárazra papírvattával majd húzzuk rá a védőt. Mosogatáshoz 2x desztillált vizet használjunk! A cellát a 2x desztillált vízzel töltsük meg, így hagyjuk ázni a következő csoport méréséig.
A
mérési adatokat az Internetről vagy a hallgatói gépterem szerveréről tölthetjük
le (részletek az oktatóktól).
- A mérési adatokat tartalmazó adatállományok
nevei
(ezek hiánya automatikusan FORMAI HIBÁ-t eredményez!); - az
oxigénredukció vizsgálata során különböző fordulatszámokon felvett görbék
egy ábrán;
- a gyakorlaton
megbeszélt potenciálnál az áram ábrázolása a fordulatszám függvényében;
- a levegő
kiűzése során felvett görbék egy ábrán;
- a
halogenid-tartalmú oldatban felvett görbe, feltüntetve hogy melyik ion hol
válik le.